همهگیری افسردگی و اضطراب در جهان
افسردگی و اضطراب شایعترین اختلالات سلامت روان در سراسر جهان هستند. حدود ۳۰۰ میلیون نفر با افسردگی و نزدیک به ۳۰۱ میلیون نفر با اختلالات اضطرابی زندگی میکنند؛ آماری که تقریباً ۸ درصد جمعیت جهان را دربر میگیرد.
با این حال، یافتن درمان مناسب برای بسیاری از بیماران، فرآیندی طولانی و گاه ناامیدکننده است. داروهای اولیهای که تجویز میشوند، اغلب کارایی لازم را ندارند. در حقیقت، نزدیک به نیمی از بیماران مبتلا به افسردگی یا اضطراب از درمان اولیه خود بهره چندانی نمیبرند و مجبور میشوند هفتهها یا ماهها داروهای مختلف را امتحان کنند تا بهبود یابند.
🧠 رویکردی ژنتیکی برای انتخاب درمان مؤثر
گروهی از پژوهشگران از آلمان، سوئد و دانمارک بر این باورند که شاید پاسخی برای این مشکل یافتهاند. آنان روشی ژنتیکی توسعه دادهاند که میتواند به پزشکان کمک کند پیشبینی کنند کدام داروی ضدافسردگی یا ضداضطراب برای هر فرد مؤثرتر است.
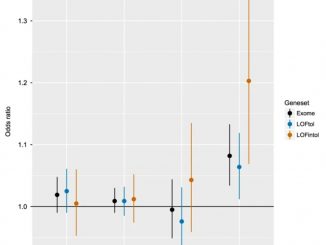
این روش بر پایهی امتیاز خطر چندژنی (Polygenic Risk Score – PRS) عمل میکند که با بررسی DNA فرد، تأثیر واریانتهای ژنتیکی بر پاسخ به داروهای خاص را ارزیابی میکند.
با انجام تنها یک تست ژنتیکی، دانشمندان قادر خواهند بود داروهایی را که بیشترین احتمال اثربخشی در هر بیمار دارند، تخمین بزنند.
اگرچه این روش تاکنون تنها با دادههای تحقیقاتی و نه بیماران واقعی آزمایش شده، نتایج اولیه بسیار امیدبخش است.
پروفسور فردریک اوس (Fredrik Åhs) از دپارتمان روانشناسی و مددکاری اجتماعی دانشگاه Mid Sweden میگوید:
«هدف ما توسعهی تستهایی هدفمندتر است. در بلندمدت، میخواهیم آزمایشی در اختیار پزشکان قرار دهیم تا بر اساس ژنهای هر فرد، داروی مناسب را انتخاب کنند. همچنین به بررسی بیومارکرها نیز علاقهمندیم. امیدواریم در آینده آزمایشی ارزان و کارآمد داشته باشیم که بتواند رنج بیماران را بسیار سریعتر کاهش دهد.»
🧩 همکاری با دانشگاه Aarhus و توسعه مدلهای ژنتیکی
این پروژه دو سال پیش آغاز شد، زمانی که پروفسور اوس با پروفسور داگ اسپید (Doug Speed) از مرکز ژنتیک کمی و ژنومیک دانشگاه Aarhus دانمارک تماس گرفت تا از مدلهای پیشرفتهی او در زمینهی امتیاز خطر چندژنی برای تحقیقات خود در درمانهای روانی بهره بگیرد.
اسپید سالهاست که در زمینهی تحلیل دادههای پیچیدهی ژنتیکی انسان فعالیت میکند، بهویژه در مورد نقش ژنها در اختلالات روانی. او توضیح میدهد:
«در ده سال گذشته، تلاش کردهایم از PRS برای پیشبینی بیماریها استفاده کنیم. این کار بسیار دشوار است، چون بسیاری از بیماریها ناشی از هزاران واریانت در سراسر ژنوم هستند. اما یافتهی جالب این است که همین امتیازهای چندژنی میتوانند پاسخ دارویی افراد را هم پیشبینی کنند؛ موضوعی که شگفتانگیز اما گامی مهم به جلوست.»
اسپید پیشتر مدلهای PRS را برای چند اختلال روانپزشکی از جمله اسکیزوفرنی، اضطراب، اختلال دوقطبی و افسردگی توسعه داده بود که همگی در این مطالعه جدید نیز بهکار گرفته شدند.
🧬 امتیاز خطر چندژنی (Polygenic Risk Score) چیست؟
پس از نقشهبرداری از ژنوم انسان در اوایل دههی ۲۰۰۰، دانشمندان هزاران تغییر کوچک در DNA را شناسایی کردند که میتواند بر سلامت اثر بگذارد. انسان حدود ۲۰ هزار ژن دارد و هر ژن در نسخههای مختلفی (alleles) وجود دارد. برخی از این نسخهها با افزایش خطر ابتلا به بیماریهای خاص مرتبط هستند.
پژوهشگرانی مانند اسپید با ترکیب این دادهها، ابزارهایی به نام امتیاز خطر چندژنی (PRS) ایجاد میکنند که اثر جمعی واریانتهای ژنتیکی مختلف را برای برآورد خطر ابتلا به یک بیماری خاص میسنجند.
برای مثال، در توسعهی PRS برای افسردگی، ژنوم فرد بررسی میشود تا مشخص شود چه تعداد از واریانتهای مرتبط با افسردگی را دارد؛ هرچه تعداد این واریانتها بیشتر باشد، امتیاز خطر ژنتیکی نیز بالاتر است. البته برخی واریانتها اثر قویتری نسبت به بقیه دارند.
👯♀️ دادههای دوقلوها: نگاهی به نقش ژنها در پاسخ دارویی
امتیازهای چندژنی بیماری را تشخیص نمیدهند، بلکه احتمال بروز آن را تخمین میزنند. اما ممکن است بتوانند توضیح دهند چرا برخی درمانها در افراد خاص مؤثرترند.
برای بررسی این موضوع، اوس و همکارانش از دادههای پایگاه ثبت دوقلوهای سوئدی (Swedish Twin Registry) استفاده کردند که بزرگترین بانک اطلاعاتی از نوع خود در جهان است. این پایگاه به پژوهشگران اجازه میدهد اثرات نسبی ژنتیک و محیط را بر سلامت و رفتار مقایسه کنند.
آنها ۲٬۵۱۵ نفر از این پایگاه را که داروهای ضدافسردگی یا ضداضطراب دریافت کرده بودند، شناسایی کردند. با بررسی نوع دارو، تغییرات نسخه و روند درمان، مشخص شد کدام داروها بیشترین اثربخشی را داشتند.
اوس میگوید:
«با بررسی امتیازهای چندژنی این افراد متوجه شدیم کسانی که امتیاز خطر ژنتیکی بالاتری برای افسردگی یا اضطراب داشتند، داروهایی مانند بنزودیازپینها و آنتیهیستامینها در آنها اثر کمتری داشتند. هنوز به پژوهشهای بیشتری نیاز داریم، اما امیدواریم در آینده بتوانیم تستهایی دقیق طراحی کنیم که پیشبینی کنند کدام دارو احتمالاً برای هر فرد مؤثرتر است.»
⚠️ محدودیتها و گامهای آینده
همانند بسیاری از مطالعات علمی، این پژوهش نیز محدودیتهایی دارد. اوس توضیح میدهد که اگرچه دادهها گسترده بودند، اما کامل نبودند:
«اطلاعات مربوط به پاسخ بیماران به داروها از روی دادههای نسخهنویسی استخراج شد، نه از یادداشتهای بالینی. بنابراین میتوان حدسهایی زد، اما نمیتوان مطمئن بود که دلیل تغییر دارو دقیقاً چه بوده است — عوارض جانبی، عدم بهبودی، یا دلیل دیگر. با این حال، نتایج ما با مطالعات بالینی دیگر سازگار بود.»
علاوه بر این، تحلیلها به بازه زمانی مشخصی محدود شد، بنابراین ممکن است نسخههای قدیمیتر در دادهها ثبت نشده باشند. اوس میافزاید:
«این موضوع احتمالاً روی تعداد افرادی که فقط یک دارو دریافت کردهاند تأثیر گذاشته است. برخی ممکن است پیشتر داروهای دیگری مصرف کرده باشند که در دادهها ثبت نشدهاند. به همین دلیل قصد داریم در آینده مطالعهی بالینی پیگیری انجام دهیم.»
🔬 به سوی روانپزشکی شخصیسازیشده
اگرچه هنوز نیاز به تحقیقات بیشتری وجود دارد، یافتههای این مطالعه نویدبخش آیندهای است که در آن انتخاب داروی ضدافسردگی دیگر بر پایهی «آزمون و خطا» نخواهد بود.
با یک تست سادهی ژنتیکی، پزشکان میتوانند از همان ابتدا درمانی را انتخاب کنند که با ساختار ژنتیکی بیمار سازگارتر است — رویکردی که میتواند زمان درمان را کاهش دهد، عوارض را کم کند و کیفیت زندگی میلیونها نفر را بهبود بخشد.
تهیه و تنظیم: سید طه نوربخش
نظارت و تأیید: فائزه محمدهاشم-متخصص ژنتیک