دانشمندان با رمزگشایی ساختار سهبعدی یک آنزیم کلیدی مرتبط با بیماری آلزایمر، افقهای تازهای را برای توسعه داروهای هدفمند و بهبود گزینههای درمانی گشودند. پژوهشگران مؤسسه تحقیقات پزشکی سنت وینسنت در ملبورن، استرالیا، موفق شدند ساختار فضایی آنزیم فسفولیپاز D3 را شناسایی کنند؛ آنزیمی که گمان میرود نقش مهمی در تنظیم پروتئین آمیلوئید بتا، از عوامل اصلی بروز آلزایمر، ایفا میکند. این یافته، مسیر تازهای برای طراحی درمانهای نوآورانه علیه آلزایمر و دیگر بیماریهای تحلیلبرنده عصبی هموار میسازد.
PLD3 (فسفولیپاز D3) و نقش آن در بیماری آلزایمر
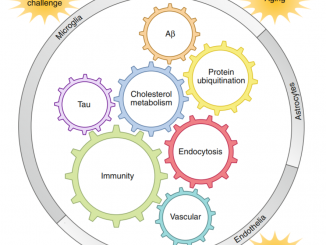
PLD3 آنزیمی دخیل در متابولیسم چربیهاست، اما اختلال عملکرد آن با انباشت پلاکهای آمیلوئید بتا در مغز ــ یکی از ویژگیهای بارز آلزایمر ــ مرتبط دانسته شده است. این پلاکهای سمی با بر هم زدن عملکرد طبیعی نورونها، به بروز اختلالات حافظه، افت شناختی و سایر علائم ناتوانکننده منجر میشوند.
جهشهای ژنتیکی در ژن PLD3 با افزایش سطح آمیلوئید بتا و تشدید تشکیل پلاکها ارتباط دارد. با اینکه PLD3 هدف بالقوهای برای مداخله درمانی بهشمار میرفت، نبود اطلاعات دقیق ساختاری، شناخت نحوه تأثیر آن بر متابولیسم آمیلوئید را دشوار کرده بود.
اکنون پژوهشگران استرالیایی با بهرهگیری از میکروسکوپ الکترونی کرایو (cryo-EM) توانستند ساختار سهبعدی PLD3 را با دقت بالا شناسایی کنند. این دستاورد، دیدگاههای ارزشمندی درباره عملکرد آنزیم و نحوه تعامل آن با سایر مولکولهای مغز فراهم کرده و گامی مهم در جهت مهار نقش بیماریزای آن در آلزایمر بهشمار میرود.
پیامدهای این کشف در توسعه دارو
اطلاعات ساختاری بهدستآمده از PLD3 اکنون امکان طراحی منطقی داروها را فراهم میسازد؛ داروهایی که یا بهصورت مولکولهای کوچک یا بیولوژیک، بتوانند عملکرد این آنزیم را تعدیل کنند. یکی از راهبردهای درمانی ممکن، تقویت عملکرد PLD3 برای کاهش تولید آمیلوئید بتا و در نتیجه، پیشگیری یا کند کردن تشکیل پلاکهاست.
علاوه بر آلزایمر، این یافتهها میتوانند در درمان دیگر بیماریهای تحلیلبرنده عصبی نیز کاربرد داشته باشند؛ بیماریهایی که در آنها مکانیسمهای آسیبشناختی مشابه، از جمله تجمع پروتئینهای سمی، نقش دارند. همین قابلیت چندمنظوره، PLD3 را به هدفی جذاب برای توسعه داروهای جدید تبدیل کرده است.
کشف ساختار PLD3 همچنین با روند روبهرشد استفاده از درمانهای ترکیبی در آلزایمر همراستا است. درمانهای کنونی، مانند آنتیبادیهای ضد آمیلوئید، زمانی که بهتنهایی استفاده میشوند، موفقیت محدودی داشتهاند. ترکیب این درمانها با داروهایی که فرایندهای پیشزمینهای مانند تنظیم آمیلوئید توسط PLD3 را هدف میگیرند، میتواند اثربخشی بیشتری به همراه داشته باشد.
پروفسور مایکل پارکر، سرپرست این مطالعه، میگوید:”این ساختار از اهمیت زیادی برخوردار است، زیرا به ما امکان میدهد مولکولهایی را طراحی کنیم که فعالیت این آنزیم را تنظیم کنند و بالقوه قابلیت تبدیل به دارو را داشته باشند. کشف ما درباره PLD3 گامی نخست در مسیر توسعه داروهای جدیدی است که میتوان آنها را همراه با درمانهای هدفمند دیگر به کار برد.”
تأثیرات گستردهتر بر پژوهشهای بیماریهای عصبی
شناسایی ساختار PLD3 نهتنها گامی مهم در فهم بهتر آلزایمر محسوب میشود، بلکه الگویی برای مطالعه آنزیمهای کمتر شناختهشده در دیگر اختلالات عصبی نیز فراهم میکند. بهکارگیری رویکردهای مشابه میتواند راه را برای درمان بیماریهایی مانند زوال اجسام لوی (Lewy body dementia) و دمانس فرونتوتمپورال هموار سازد.
اکنون با در دست داشتن ساختار PLD3، پژوهشگران قصد دارند غربالگری گستردهای برای یافتن ترکیبات دارویی مناسب آغاز کنند. همکاری با شرکتهای دارویی میتواند روند تبدیل این کشف به درمانهای عملی را سرعت ببخشد.
این پیشرفت، نقطه عطفی در مسیر مبارزه با آلزایمر به شمار میرود و در حالی که امید تازهای برای بیماران و خانوادههای آنان ایجاد کرده، زمینهساز پیشرفتهای بیشتر در حوزه پژوهشهای بیماریهای تحلیلبرنده عصبی نیز خواهد بود.
منبع:
Crystal structure of Alzheimer’s disease phospholipase D3 provides a molecular basis for understanding its normal and pathological functions. https://doi.org/10.1111/febs.17277
تهیه و تنظیم: سید طه نوربخش
نظات و تأیید: فائزه محمدهاشم-متخصص ژنتیک