شکاف لب و شکاف کام از شایعترین ناهنجاریهای مادرزادی هستند و در ایالات متحده تقریباً از هر ۱۰۵۰ تولد، یک مورد را شامل میشوند. این ناهنجاریها زمانی رخ میدهند که بافتهای تشکیلدهندهی لب یا سقف دهان بهدرستی به یکدیگر نپیوندند. تاکنون این وضعیت ترکیبی از عوامل ژنتیکی و محیطی در نظر گرفته میشد. اکنون، زیستشناسان MIT دریافتهاند که چگونه یک واریانت ژنتیکی که اغلب در افراد مبتلا به این ناهنجاریهای صورت دیده میشود، منجر به بروز شکاف لب و کام میشود.
یافتههای این پژوهش نشان میدهد که این واریانت، باعث کاهش میزان مولکول RNA ناقل (tRNA ) در سلولها میشود؛ مولکولی که برای ساخت پروتئینها نقش حیاتی دارد. در نتیجه، سلولهای جنینی مسئول شکلگیری صورت نمیتوانند بهدرستی به هم متصل شوند تا ساختار کامل لب و سقف دهان را تشکیل دهند.
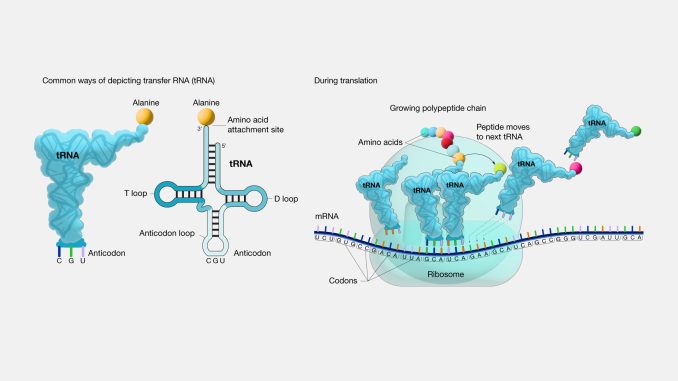
دکتر «میکائلا بارتوسل»، پژوهشگر MIT و نویسنده اول این مطالعه میگوید:”تا امروز هیچکس ارتباطی که ما کشف کردیم را مطرح نکرده بود. ژنی که بررسی کردیم—به نام DDX1—پیشتر بهعنوان یکی از اجزای درگیر در برش tRNA شناخته شده بود، اما نقش حیاتی آن در این فرآیند و همچنین در رشد صورت روشن نبود. بدون این ژن، برخی tRNAها نمیتوانند آمینواسیدها را به ریبوزوم منتقل کنند، و زمانی که tRNA درست پردازش نشود، تولید پروتئین مختل میشود.”
بررسی واریانتهای ژنتیکی
شکاف لب و کام که تحت عنوان کلی “شکافهای اوروفاسیال” نیز شناخته میشوند، ممکن است به دلایل ژنتیکی یا محیطی ایجاد شوند. اما در بسیاری از موارد علت ژنتیکی روشنی برای آنها یافت نشده است.
کالو (نویسنده مسئول مقاله حاصل از این پژوهش) توضیح میدهد: “از آنجایی که هم ژنها و هم عوامل محیطی در ایجاد شکاف کام و لب نقش دارند، سازوکار دقیق بروز این شکافها هنوز بهخوبی شناخته نشده است. در چنین شرایطی، یافتن عامل مشخص بسیار دشوار است.”
برای شناسایی عوامل ژنتیکی مؤثر، پژوهشگران اغلب از مطالعات موسوم به “بررسی همبستگی کل ژنوم (GWAS)”استفاده میکنند. در مورد شکافهای اوروفاسیال، برخی واریانتهای ژنتیکی مرتبط در نواحی غیرکدکنندهی DNA پیدا شدهاند—یعنی بخشهایی که مستقیماً پروتئینی نمیسازند.
مطالعهی MIT نشان داد این واریانتها در ناحیهای تقویتکننده (Enhancer) به نام e2p24.2 قرار دارند. این تقویتکنندهها با ژنهای مجاور در تعاملاند و با اتصال به فاکتورهای رونویسی، آنها را فعال میکنند. در این مورد خاص، محققان تمرکز خود را بر ژن DDX1 قرار دادند.
نقش DDX1 در پردازش tRNA
ژن DDX1 در برش tRNAها نقش کلیدی دارد. tRNAها آمینواسیدهای خاص را به ریبوزوم منتقل میکنند تا بر اساس دستورالعمل RNA پیامرسان، پروتئینها ساخته شوند. اگرچه حدود ۴۰۰ نوع tRNA در ژنوم انسان یافت میشود، فقط بخشی از آنها نیاز به فرآیند برش دارند—و این همان دستهای است که بیشترین تأثیر را از فقدان DDX1 میپذیرد. بهطور خاص، tRNAهای وابسته به چهار نوع آمینواسید دچار اختلال میشوند. فرضیهی پژوهشگران این است که این چهار آمینواسید در ساخت پروتئینهایی که برای رشد سلولهای صورت ضروریاند، نقش بسزایی دارند. اگر ریبوزومها نتوانند این آمینواسیدها را دریافت کنند، ساخت پروتئین متوقف میشود.
پژوهشگران اکنون در حال بررسی این موضوعاند که کدام پروتئینها بیش از همه از این اختلال آسیب میبینند و چگونه توقف ریبوزومی ممکن است منجر به فعالسازی سیگنالهای استرس در سلولها شود.
tRNA و ناهنجاریهای عصبی
این اولین مطالعهای است که tRNA را مستقیماً با ناهنجاریهای جمجمهصورتی مرتبط میسازد. با این حال، پیشتر نشان داده شده بود که اختلال در ریبوزومسازی یا سنتز tRNA میتواند باعث بروز بیماریهای عصبی-رشدی شود.
کالو میگوید:”یکی از نکات جالب این است که سلولهای سازندهی صورت و سلولهای عصبی منشأ جنینی مشترکی دارند، و به همین دلیل احتمال دارد هر دو دسته نسبت به اختلال در مسیر tRNA آسیبپذیر باشند.”
ارتباط با عوامل محیطی
محققان همچنین در حال بررسی این موضوع هستند که آیا عوامل محیطی مؤثر در شکافهای مادرزادی نیز میتوانند عملکرد tRNA را مختل کنند. شواهد اولیه نشان میدهد که استرس اکسیداتیو (تجمع رادیکالهای آزاد) میتواند به تکهتکه شدن tRNA منجر شود. این وضعیت ممکن است در اثر قرار گرفتن جنین در معرض الکل (سندرم جنین الکلی) یا ابتلای مادر به دیابت بارداری رخ دهد.
بارتوسل میگوید:” در آینده، قصد داریم هم به جستجوی جهشهای ژنتیکی بپردازیم و هم عوامل محیطی را بررسی کنیم تا بفهمیم چه چیزی میتواند از اختلال در عملکرد tRNA جلوگیری کند.”
منبع:
A non-syndromic orofacial cleft risk locus links tRNA splicing defects to neural crest cell pathologies. The American Journal of Human Genetics, 2025; DOI: 10.1016/j.ajhg.2025.03.017
تهیه و تنظیم: سید طه نوربخش
نظارت و تأیید: فائزه محمدهاشم-متخصص ژنتیک



