🔹 چالش یک فرض قدیمی
برای مدت طولانی تصور میشد که چربی موجود در مغز در بیماریهای نورودژنراتیو نقشی ندارد؛ اما پژوهشگران دانشگاه پردو این باور را به چالش کشیدهاند.
یافتههای منتشرشده در مجله Immunity نشان میدهد که تجمع چربی در سلولهای ایمنی مقیم مغز، یعنی میکروگلیا، توانایی آنها در مقابله با بیماری را مختل میکند. این کشف مسیر جدیدی را برای درمانهای نورواِمیون مبتنی بر زیستشناسی لیپیدها باز میکند؛ درمانهایی که میتوانند با بهبود عملکرد میکروگلیا و سلامت نورونی، بیماریهایی مانند آلزایمر را هدف قرار دهند. این پژوهش به رهبری گوراو چوپرا، استاد شیمی و علوم کامپیوتر در دانشگاه پردو انجام شد.
🔹 تمرکز بر سلولهای غنی از چربی، نه فقط پلاکها و کلافههای پروتئینی
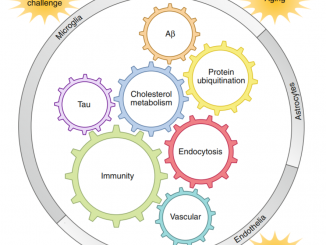
در حالی که بیشتر داروهای در حال توسعه برای آلزایمر بر پلاکهای آمیلوئید بتا و کلافههای پروتئینی تائو تمرکز دارند، چوپرا بر سلولهای غیرطبیعی غنی از چربی واقع در نواحی بیمار مغز متمرکز است.
در پژوهشهای پیشین منتشرشده در Nature، چوپرا و همکارانش نشان دادند که آستروسیتها—نوع دیگری از سلولهای پشتیبان نورونها—در شرایط بیماری اسید چرب سمی آزاد میکنند. در همکاری دیگری با دانشگاه پنسیلوانیا (منتشرشده در Nature سال گذشته)، مشخص شد که اختلال عملکرد میتوکندریایی در نورونها با رسوبات چربی در سلولهای گلیال طی افزایش سن—یکی از عوامل اصلی خطر نورودژنراسیون—ارتباط دارد.
چوپرا میگوید:
«به نظر ما هدف قرار دادن مستقیم پلاکها یا کلافهها مشکل را حل نمیکند؛ باید عملکرد سلولهای ایمنی مغز را بازیابی کنیم. ما درمییابیم که کاهش تجمع چربی در مغز بیمار کلید ماجراست، زیرا چربی انباشتهشده کار سیستم ایمنی را دشوار میکند. با هدف قرار دادن این مسیرها میتوانیم توانایی میکروگلیا برای مقابله با بیماری و حفظ تعادل مغز را بازگردانیم.»
🔹 همکاریهای تحقیقاتی و زمینه علمی
تیم چوپرا با پژوهشگران کلینیک کلیولند به رهبری دیمیتریوس داوالوس همکاری کرد. چوپرا همچنین عضو چندین مؤسسه تحقیقاتی دانشگاه پردو است، از جمله مرکز اکتشاف دارو، مؤسسه علوم اعصاب یکپارچه و مرکز مهندسی مراقبت سلامت.
این کار بخشی از ابتکار «وان هلث» ریاست دانشگاه پردو است که سلامت انسان، حیوان و گیاه را به هم پیوند میدهد و بر توسعه روشهای شیمی پیشرفته تمرکز دارد.
🔹 بازخوانی سرنخهای تاریخی
بیش از ۱۰۰ سال پیش، آلویس آلزایمر در مغز بیماری که این اختلال به نام او ثبت شده است، پلاکها، کلافهها و سلولهای حاوی قطرات چربی را مشاهده کرد؛ اما برای سالها این قطرات چربی بیاهمیت تلقی میشدند.
اما ارتباطهایی که تیم چوپرا میان بیماریهای نورودژنراتیو و چربی در میکروگلیا و آستروسیتها نشان داده، خلاف این تصور را ثابت میکند. چوپرا میگوید این یافتهها پایهای برای «مدل لیپیدی جدید نورودژنراسیون» فراهم میکند. او این تجمعات چربی را «پلاکهای لیپیدی» مینامد.
«مشکل خودِ قطرات چربی نیست، بلکه تجمع آنهاست که بیماریزاست. ترکیب مولکولی این لیپیدهای انباشتهشده احتمالاً یکی از محرکهای اصلی التهاب عصبی و بیماریهایی مانند آلزایمر است.»
🔹میکروگلیا چگونه آسیب میبیند؟
میکروگلیا سلولهای ایمنی واقعی مغز هستند که بقایای سلولی و پروتئینهای ناصحیح تاخورده مانند آمیلوئید بتا و تائو را با فرآیند فاگوسیتوز پاکسازی میکنند.
تیم چوپرا با بررسی میکروگلیا در حضور آمیلوئید بتا دریافت:
- در بافت مغزی بیماران آلزایمر، میکروگلیا نزدیک پلاکها دو برابر چربی بیشتری نسبت به میکروگلیاهای دورتر دارند.
- میکروگلیای دارای قطرات چربی، ۴۰٪ کمتر آمیلوئید بتا را پاکسازی میکنند.
پژوهشها نشان داد که میکروگلیا در تماس با پلاکها اسیدهای چرب آزادِ اضافی تولید میکنند. در حالت طبیعی مقدار کمی از این اسیدهای چرب به عنوان انرژی استفاده میشود؛ اما میکروگلیاهای نزدیک پلاکها این اسیدهای چرب را به تریاسیلگلیسرول تبدیل میکنند و چربی بیش از حد ذخیره میشود.
این روند با سن و پیشرفت بیماری شدت میگیرد.
🔹 یافتن عامل کلیدی: آنزیمی که تخریب نمیشود
تیم پژوهشی مسیر تبدیل اسیدهای چرب به تریاسیلگلیسرول را دنبال کرد و روی مرحله نهایی این فرآیند متمرکز شد.
نتیجه:
- سطح یک آنزیم به نام DGAT2 به شکل غیرطبیعی بالا بود.
- اما ژن DGAT2 افزایش نداشت؛ مشکل از تولید نبود، از تخریبنشدن آنزیم بود.
انباشت آنزیم DGAT2 باعث میشود میکروگلیا اسیدهای چرب را وارد مسیر ذخیرهسازی کند—نه انرژیسازی یا ترمیم—و به همین دلیل از کار بیفتد.
چوپرا میگوید:
«نشان دادیم که آمیلوئید بتا مستقیماً مسئول تشکیل چربی داخل میکروگلیا است. این رسوبات باعث اختلال عملکرد میکروگلیا و توقف پاکسازی آمیلوئید بتا میشوند.»
🔹 یک مسیر درمانی جدید: هدف قرار دادن DGAT2
پژوهشگران دو مولکول را آزمودند: یکی مهارکننده عملکرد DGAT2 و دیگری تسهیلکننده تجزیه آن.
نتیجه در مدلهای حیوانی آلزایمر:
- کاهش چربی مغزی
- بهبود عملکرد میکروگلیا
- افزایش توانایی آنها در پاکسازی پلاکها
- بهبود سلامت نورونی
چوپرا میگوید:
«وقتی آنزیم تولیدکننده چربی را مهار یا حذف میکنیم، توانایی میکروگلیا برای مبارزه با بیماری و حفظ تعادل مغز بازمیگردد.»
نویسندگان همکار نیز میگویند که این یافتهها مسیر درمانی کاملاً جدیدی را معرفی میکند:
بازگرداندن متابولیسم میکروگلیا → بازگرداندن دفاع طبیعی مغز.
منبع:
1-Priya Prakash, Palak Manchanda, Evi Paouri, Kanchan Bisht, Kaushik Sharma, Jitika Rajpoot, Victoria Wendt, Ahad Hossain, Prageeth R. Wijewardhane, Caitlin E. Randolph, Yihao Chen, Sarah Stanko, Nadia Gasmi, Anxhela Gjojdeshi, Sophie Card, Jonathan Fine, Krupal P. Jethava, Matthew G. Clark, Bin Dong, Seohee Ma, Alexis Crockett, Elizabeth A. Thayer, Marlo Nicolas, Ryann Davis, Dhruv Hardikar, Daniela Allende, Richard A. Prayson, Chi Zhang, Dimitrios Davalos, Gaurav Chopra. Amyloid-β induces lipid droplet-mediated microglial dysfunction via the enzyme DGAT2 in Alzheimer’s disease. Immunity, 2025; 58 (6): 1536 DOI: 10.1016/j.immuni.2025.04.029 Kevin A.
2-Guttenplan, Maya K. Weigel, Priya Prakash, Prageeth R. Wijewardhane, Philip Hasel, Uriel Rufen-Blanchette, Alexandra E. Münch, Jacob A. Blum, Jonathan Fine, Mikaela C. Neal, Kimberley D. Bruce, Aaron D. Gitler, Gaurav Chopra, Shane A. Liddelow, Ben A. Barres. Neurotoxic reactive astrocytes induce cell death via saturated lipids. Nature, 2021; 599 (7883): 102 DOI: 10.1038/s41586-021-03960-y
3-China N. Byrns, Alexandra E. Perlegos, Karl N. Miller, Zhecheng Jin, Faith R. Carranza, Palak Manchandra, Connor H. Beveridge, Caitlin E. Randolph, V. Sai Chaluvadi, Shirley L. Zhang, Ananth R. Srinivasan, F. C. Bennett, Amita Sehgal, Peter D. Adams, Gaurav Chopra, Nancy M. Bonini. Senescent glia link mitochondrial dysfunction and lipid accumulation. Nature, 2024; 630 (8016): 475 DOI: 10.1038/s41586-024-07516-8
تهیه و تنظیم: سید طه نوربخش
نظارت و تأیید: فائزه محمدهاشم-متخصص ژنتیک